La Agencia Europea de Medicamentos ofrece prácticas para graduados universitarios en su sede de Ámsterdam, Países Bajos. El objetivo es que los becarios comprendan el funcionamiento de la Agencia y su papel en la UE. El programa se desarrolla del 1 de octubre al 31 de julio de cada año. Requisitos: Recién graduados universitarios (hasta […]
Empleo – Jefe del Servicio del Puesto de Trabajo Digital – Países Bajos
La Agencia Europea de Medicamentos (EMA) busca un jefe de equipo dinámico y con experiencia para incorporarse a la división de Gestión de la Información como Jefe del Servicio de Puesto de Trabajo Digital. Este puesto dependerá directamente del Jefe del Departamento de Servicios Centrales y será responsable de liderar y mejorar nuestra gestión de […]
Prácticas en la Agencia Europea de Medicamentos
La Agencia Europea de Medicamentos ofrece periodos de prácticas para titulados universitarios en su sede de Ámsterdam (Países Bajos). El objetivo es que los becarios conozcan la Agencia y su papel en la UE. El programa se desarrolla del 1 de octubre al 31 de julio de cada año. Quién puede optar titulados universitarios recientes […]
COVID-19: La Comisión Europea autoriza una segunda vacuna adaptada para las campañas de vacunación de otoño
La Comisión ha autorizado la vacuna Spikevax XBB.1.5 adaptada a COVID-19, desarrollada por Moderna. Se trata de otro paso importante en la lucha contra la enfermedad. Es la tercera adaptación de esta vacuna para responder a las nuevas variantes de COVID-19. La Agencia Europea de Medicamentos (EMA) llevó a cabo una rigurosa evaluación de la […]
Unión Europea de la Salud: refuerzo de la respuesta sanitaria de la UE
El Consejo ha adoptado hoy los últimos componentes de la Unión Europea de la Salud: el Reglamento sobre las amenazas transfronterizas graves para la salud, el Reglamento sobre el mandato ampliado del Centro Europeo para la Prevención y el Control de las Enfermedades (ECDC) y el Reglamento marco de emergencia destinado a otorgar competencias adicionales a la Autoridad Europea […]
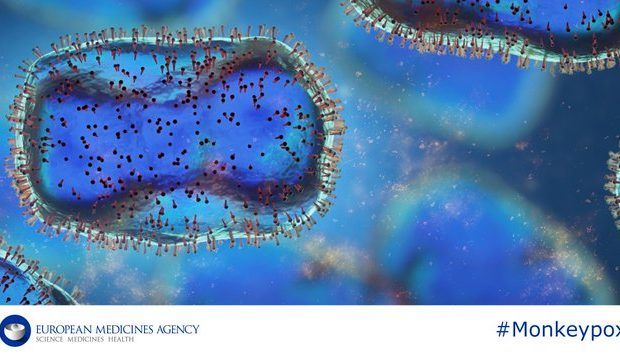
La EMA aconseja el uso intradérmico de la vacuna contra la viruela del mono
La Agencia Europea de Medicamentos (EMA) ha aconsejado el uso intradérmico de la vacuna contra la viruela del mono. El Grupo de Trabajo de Emergencia (ETF) de la EMA ha revisado los datos que muestran que las personas que recibieron la vacuna contra la viruela del mono como inyección intradérmica (inyección en la piel) producen […]
Respuesta de la EMA a la emergencia de salud pública causada por la viruela del mono
La Agencia Europea de Medicamentos (EMA) ha iniciado una serie de acciones para responder al actual brote de viruela del mono, que fue elevado por la Organización Mundial de la Salud (OMS) a Emergencia de Salud Pública de Importancia Internacional (PHEIC) el sábado 23 de julio. Se trata de la primera nueva PHEIC que se […]
Declaración de la presidenta von der Leyen con el presidente del Gobierno de España, Pedro Sánchez
Querido Presidente, querido Pedro: Me complace verte aquí. Este es un momento muy especial, porque hoy es un día histórico para las relaciones entre la Unión Europea y los países de América Latina y el Caribe. Porque ponemos en marcha una nueva asociación para vacunas y medicamentos fabricados en América Latina, para los latinoamericanos, con […]
Inicio de la revisión continua de la vacuna adaptada Spikevax COVID-19
La EMA ha iniciado una revisión continua de una versión de Spikevax adaptada para proporcionar una mejor protección contra variantes específicas del SARS-CoV-2, el virus que causa el COVID-19. La revisión se refiere a una vacuna bivalente. Esto significa que se dirigirá a dos cepas de SARS-CoV-2, en este caso la cepa original y la […]