La Agencia Europea de Medicamentos (EMA) ha iniciado una serie de acciones para responder al actual brote de viruela del mono, que fue elevado por la Organización Mundial de la Salud (OMS) a Emergencia de Salud Pública de Importancia Internacional (PHEIC) el sábado 23 de julio.
Se trata de la primera nueva PHEIC que se declara desde que es aplicable el reglamento que refuerza el papel de la EMA en la preparación y gestión de crisis de medicamentos y productos sanitarios.
Desde el comienzo del reciente brote de viruela del mono, la EMA ha seguido de cerca la situación y ya ha tomado múltiples medidas para preparar y apoyar la respuesta de la UE. Esto incluye la recomendación de la Agencia el 22 de julio de aprobar una ampliación de la indicación de la vacuna Imvanex para proteger a los adultos de la enfermedad de la viruela del mono. Los nuevos poderes otorgados a la Agencia en virtud de su mandato ampliado desencadenan actividades adicionales ahora que la viruela del mono ha sido declarada emergencia de salud pública.
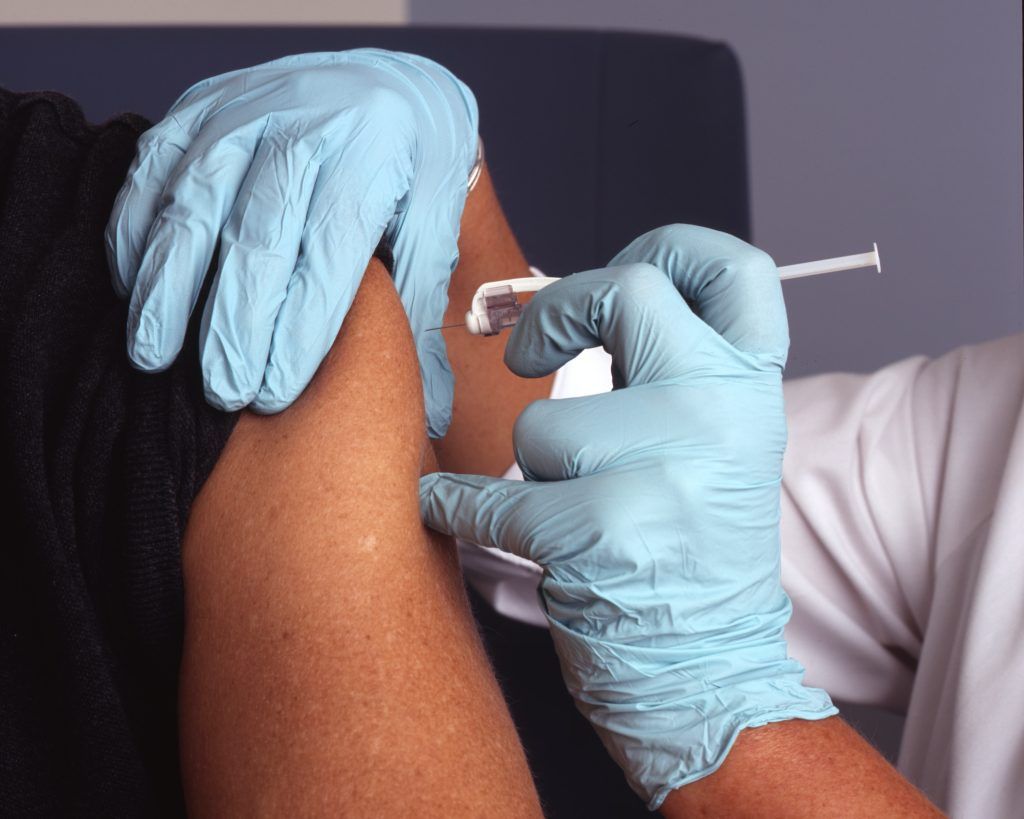
Comienza la entrega de vacunas en respuesta al brote de viruela del mono
|
Seguimiento de la oferta, la demanda y el desabastecimiento de medicamentos
El Grupo Directivo Ejecutivo de la EMA sobre Desabastecimiento y Seguridad de los Medicamentos (MSSG), creado por el nuevo Reglamento, elaborará y mantendrá una lista formal de medicamentos críticos para la emergencia de salud pública relacionada con la viruela del mono. La lista se elaborará en un proceso de colaboración en el que participarán los Estados miembros, los profesionales sanitarios, los pacientes y los consumidores.
Los titulares de las autorizaciones de comercialización de los medicamentos incluidos en la lista deberán actualizar periódicamente a la EMA la información pertinente sobre la escasez potencial o real y las existencias disponibles, así como las previsiones de oferta y demanda. Además, los Estados miembros proporcionarán informes periódicos sobre la demanda estimada de estos medicamentos a nivel nacional.
Esto permitirá al MSSG recomendar y coordinar las acciones apropiadas a nivel de la UE a la Comisión Europea y a los Estados miembros de la UE con el fin de prevenir o mitigar la escasez potencial o real de medicamentos críticos para salvaguardar la salud pública.
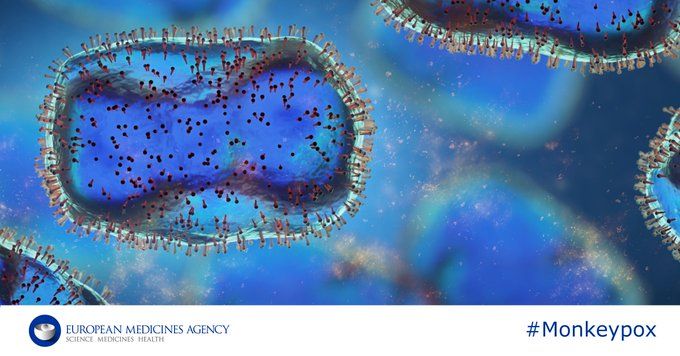
Evolución de la viruela del mono en Europa
|
Actualmente hay dos medicamentos autorizados específicamente para la viruela del mono en la UE:
- El medicamento Tecovirimat SIGA está autorizado para el tratamiento de la viruela, la viruela del mono y la viruela vacuna.
- La vacuna Imvanex está autorizada para proteger a los adultos contra la viruela y la viruela del mono. Imvanex se comercializa como Jynneos en los EE.UU. y, teniendo en cuenta la limitada disponibilidad de Imvanex, la ETF ha recomendado que Jynneos pueda utilizarse para proporcionar protección contra la viruela del mono en la UE.
Más información: Agencia Europea del Medicamento – Comunicado de prensa




Deja una respuesta