El Comité de Medicamentos de Uso Humano (CHMP) de la EMA ha recomendado que se amplíe la indicación de la vacuna COVID-19 Comirnaty para incluir su uso en niños de 12 a 15 años. La vacuna ya está aprobada para su uso en adultos y adolescentes de 16 años o más.
Comirnaty es una vacuna para prevenir el COVID-19. Contiene una molécula llamada ARN mensajero (ARNm) con instrucciones para producir una proteína, conocida como proteína de espiga, presente de forma natural en el SARS-CoV-2, el virus que causa la COVID-19. La vacuna actúa preparando al organismo para defenderse del SARS-CoV-2.
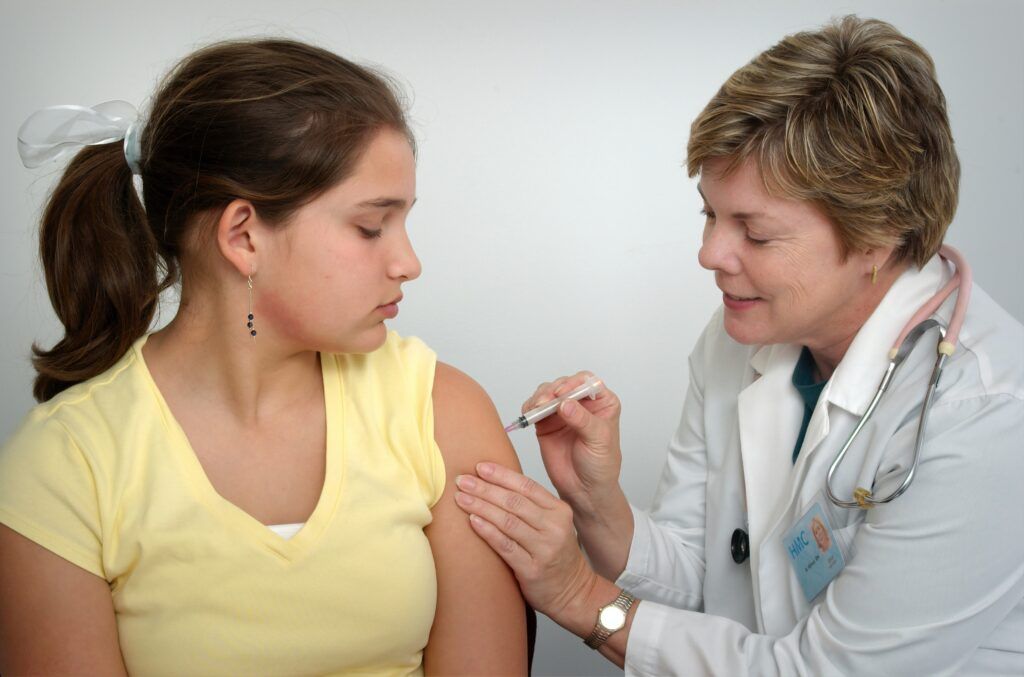
El uso de la vacuna Comirnaty en los niños de 12 a 15 años será el mismo que en los mayores de 16 años. Se administra en forma de dos inyecciones en los músculos de la parte superior del brazo, con un intervalo de tres semanas.
Los efectos de Comirnaty en los niños se investigaron en 2.260 niños de 12 a 15 años. Este estudio se llevó a cabo de acuerdo con el plan de investigación pediátrica (PIP) de Comirnaty, que fue aprobado por el Comité Pediátrico de la EMA (PDCO).
El ensayo demostró que la respuesta inmunitaria a Comirnaty en este grupo era comparable a la respuesta inmunitaria en el grupo de edad de 16 a 25 años (medida por el nivel de anticuerpos contra el SARS-CoV-2). La eficacia de Comirnaty se calculó en cerca de 2.000 niños de 12 a 15 años que no tenían signos de infección previa. Éstos recibieron la vacuna o un placebo (una inyección ficticia), sin saber cuál se les administró. De los 1.005 niños que recibieron la vacuna, ninguno desarrolló COVID-19, en comparación con 16 niños de los 978 que recibieron la inyección ficticia. Esto significa que, en este estudio, la vacuna fue 100% efectiva para prevenir la COVID-19 (aunque la tasa real podría estar entre el 75% y el 100%).
Los efectos secundarios más comunes en los niños de 12 a 15 años son similares a los de los mayores de 16 años. Incluyen dolor en el lugar de la inyección, cansancio, dolor de cabeza, dolor muscular y articular, escalofríos y fiebre. Estos efectos suelen ser leves o moderados y mejoran a los pocos días de la vacunación.
El CHMP concluyó que los beneficios de Comirnaty en este grupo de edad superan los riesgos.
El CHMP señaló que, debido al limitado número de niños incluidos en el estudio, el ensayo no podría haber detectado efectos secundarios poco frecuentes. El comité también señaló que el comité de seguridad PRAC de la EMA está evaluando actualmente casos muy raros de miocarditis (inflamación del músculo cardíaco) y pericarditis (inflamación de la membrana que rodea el corazón) que se produjeron tras la vacunación con Comirnaty, principalmente en personas menores de 30 años. Actualmente no hay indicios de que estos casos se deban a la vacuna y la EMA está vigilando de cerca esta cuestión.
A pesar de esta incertidumbre, el CHMP consideró que los beneficios de Comirnaty en niños de 12 a 15 años superan los riesgos, en particular en niños con condiciones que aumentan el riesgo de COVID-19 grave.
La seguridad y la eficacia de la vacuna, tanto en niños como en adultos, seguirán siendo objeto de un estrecho seguimiento a medida que se utilice en las campañas de vacunación en los Estados miembros, a través del sistema de farmacovigilancia de la UE y de los estudios en curso y adicionales realizados por la empresa y por las autoridades europeas.
¿Cómo funciona Comirnaty?
Comirnaty actúa preparando al organismo para defenderse del COVID-19. Contiene una molécula llamada ARN mensajero (ARNm) que tiene instrucciones para fabricar la proteína spike. Ésta es una proteína de la superficie del virus del SRAS-CoV-2 que el virus necesita para entrar en las células del organismo.
Cuando una persona recibe la vacuna, algunas de sus células leerán las instrucciones del ARNm y producirán temporalmente la proteína spike. El sistema inmunitario de la persona reconocerá entonces esta proteína como extraña y producirá anticuerpos y activará las células T (glóbulos blancos) para que la ataquen.
Si, más adelante, la persona entra en contacto con el virus del SRAS-CoV-2, su sistema inmunitario lo reconocerá y estará preparado para defender al organismo contra él.
El ARNm de la vacuna no permanece en el organismo, sino que se descompone poco después de la vacunación.



Deja una respuesta